جواب باهم بیندیشیم صفحه ۱۰۶ و ۱۰۷ شیمی دوازدهم تجربی و ریاضی ؛ در این مقاله به پاسخ و جواب سوالات تمرین با هم بیندیشیم صفحه ی 106 و 107 فصل چهارم شیمی راهی به سوی آیندهای روشن کتاب شیمی دوازدهم تجربی و ریاضی فیزیک متوسطه دوم پرداخته ایم. در ادامه با بخش آموزش و پرورش ماگرتا همراه ما باشید.
همچنین بخوانید: جواب خود را بیازمایید صفحه ۱۰۵ شیمی دوازدهم

پاسخ و حل با هم بیندیشیم صفحه ۱۰۶ و ۱۰۷ شیمی دوازدهم تجربی و ریاضی
۱- جدول داده شده اثر دما را بر ثابت تعادل زیر نشان میدهد. با توجه به آن به پرسشها پاسخ دهید.
2SO3(g) ⇌ 2SO2(g) + O2(g)
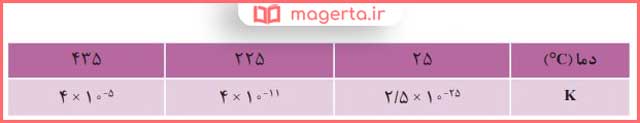
آ) عبارت ثابت تعادل را برای آن بنویسید.
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

ب) میزان پیشرفت واکنش در کدام دما بیشتر است؟ چرا؟
پاسخ: دمای 435 درجه ، زیرا ثابت تعادل در این دما عدد بزرگتری است. به این معنا که واکنش در این دما به سمت تولید فراورده، پیشرفت بیشتری داشته است.
پ) با افزایش دما K چه تغییری کرده است؟ این تغییر، جابه جا شدن تعادل را در چه جهتی نشان میدهد؟
پاسخ: با افزایش دما K بزرگتر شده است، یعنی تعادل در جهت واکنش رفت جابهجا شده است.
ت) اگر برای این واکنش ΔH > 0 باشد، جا به جا شدن تعادل و افزایش K را به کمک اصل لوشاتلیه توجیه کنید.
پاسخ: با افزایش دما و بزرگتر شدن K متوجه میشویم که تعادل گرماگیر است.
طبق اصل لوشاتلیه ← با افزایش دما (T) واکنش به سمت مصرف گرما پیش میرود و تعادل به سمت واکنش گرماگیر جابهجا میشود، یعنی تعادل به سمت واکنش رفت پیش میرود.
۲- با خط زدن واژه نادرست در هر مورد، عبارت زیر را کامل کنید.
پاسخ: در زیر واژه درست را با رنگ آبی و واژه نادرست را با خط زدن مشخص کرده ایم.
هنگامی که دمای یک سامانه تعادلی افزایش مییابد، واکنش در جهت (مصرف / تولید) گرما پیش میرود، اگر این واکنش گرماگیر باشد مقدار (فراوردهها / واکنش دهندهها) در سامانه کاهش مییابد.
۳- نمودار زیر درصد مولی آمونیاک را برای سامانه تعادلی زیر در فشار ثابت نشان میدهد. باتوجه به آن به پرسشها پاسخ دهید.
N2(g) + 3H2(g) ⇌ 2NH3(g)
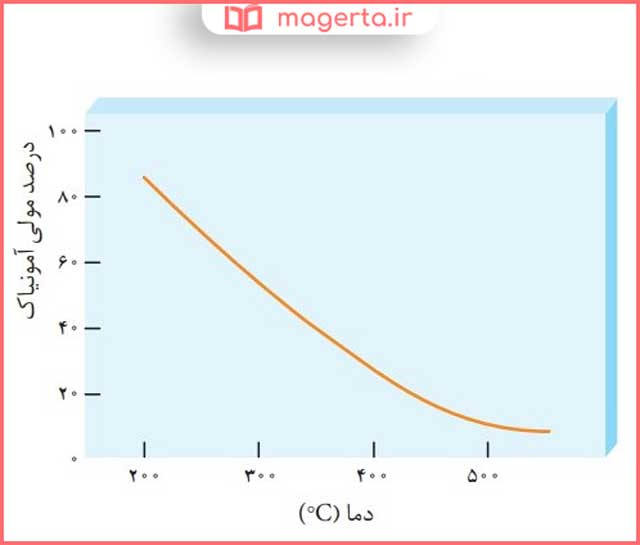
آ) با افزایش دما درصد مولی آمونیاک در سامانه چه تغییری میکند؟
پاسخ: کاهش مییابد.
ب) این واکنش گرماده است یا گرماگیر؟ چرا؟
پاسخ: گرماده ، زیرا با افزایش دما واکنش در جهت مصرف آمونیاک یعنی در جهت برگشت جا به جا شده است، پس q در سمت راست معادله قرار دارد و واکنش گرماده است.
N2(g) + 3H2(g) ⇌ 2NH3(g) + q
پ) مقدار ثابت تعادل آن در سه دمای 25 ، 200 و 400 درجه سلسیوس به صورت زیر است.
K1 = 6/2 × 10-4 , K2 = 2/24 , K3 = 6/0 × 105
کدام یک، ثابت تعادل را در دمای اتاق نشان میدهد؟ توضیح دهید.
پاسخ: K1 ، مطابق نمودار در دمای اتاق درصد مولی آمونیاک بسیار ناچیز است، پس واکنش پیشرفت کمی داشته و K تعادل باید بسیار کوچک باشد.
همچنین بخوانید: جواب خود را بیازمایید صفحه ۱۰۳ شیمی دوازدهم
توجه: شما دانش آموز پایه دوازدهم رشته های نظری ریاضی فیزیک و تجربی می توانید برای دسترسی سریع و آسان تر به جواب تمرینات و سوالات فصل های اول تا چهارم کتاب شیمی دوازدهم متوسطه دوم ، در انتهای عنوان خود عبارت «ماگرتا» را نیز در گوگل جستجو کنید.
✅ در انتها امیدواریم که مقاله توضیح و جواب سوال های با هم بیندیشیم صفحه ۱۰۶ و ۱۰۷ فصل چهارم شیمی دوازدهم تجربی و ریاضی ؛ برای شما دانش آموزان عزیز مفید بوده باشد. سوالات خود را در بخش نظرات بیان کنید.












