جواب خود را بیازمایید صفحه ۸۲ و ۸۳ شیمی یازدهم تجربی و ریاضی ؛ در این مقاله به پاسخ و جواب سوالات تمرین خودرابیازمایید صفحه ی 82 و 83 فصل دوم در پی غذای سالم کتاب شیمی یازدهم تجربی و ریاضی فیزیک متوسطه دوم پرداخته ایم. در ادامه با بخش آموزش و پرورش ماگرتا همراه ما باشید.
بعدی: جواب پیوند با ریاضی صفحه ۸۴ و ۸۵ شیمی یازدهم
جواب خود را بیازمایید صفحه ۸۶ شیمی یازدهم
جواب باهم بیندیشیم صفحه ۸۷ و ۸۸ شیمی یازدهم
جواب خود را بیازمایید صفحه ۸۹ و ۹۰ شیمی یازدهم
جواب در میان تارنماها صفحه ۹۱ شیمی یازدهم

پاسخ و حل خود را بیازمایید صفحه ۸۲ و ۸۳ شیمی یازدهم تجربی و ریاضی
در هر یک از موارد زیر با توجه به شکل، علت اختلاف در سرعت واکنش را توضیح دهید.
الف) فلزهای قلیایی سدیم و پتاسیم در شرایط یکسان با آب سرد به شدت واکنش میدهند، اما سرعت واکنشها متفاوت است.
پاسخ: واکنش پذیری پتاسیم بیش تر از سدیم است.
واکنش پذیری در گروه فلزات قلیایی با افزایش عدد اتمی افزایش می یابد.
پاسخ دیگر: هر دو فلز پتاسیم و سدیم در گروه ۱ جدول تناوبی قرار دارند، اما پتاسیم به دلیل موقعیتش در جدول، واکنشپذیری بیشتری نسبت به سدیم دارد. در یک گروه از فلزات، فعالیت شیمیایی از بالا به پایین افزایش مییابد. بنابراین، پتاسیم با عدد اتمی ۱۹ که در جایگاه پایینتری نسبت به سدیم با عدد اتمی 11 قرار دارد، دارای فعالیت شیمیایی بیشتری است.

ب) شعله آتش، گردِ آهن موجود در کپسول چینی را داغ و سرخ میکند؛ در حالی که پاشیدن و پخش کردن گردِ آهن بر روی شعله، سبب سوختن آن میشود.
پاسخ: در گرد آهن سطح تماس واکنش دهنده ها بیش تر است و سرعت واکنش بیش تر است.
پاسخ دیگر: عامل مؤثر در افزایش سرعت سوختن آهن هنگام پاشیدن گرد آهن روی شعله آتش، افزایش سطح تماس ماده فعال است. زمانی که آهن به صورت گرد پاشیده میشود، فضای بین ذرات افزایش مییابد. این امر باعث میشود که سطح تماس ذرات آهن با اکسیژن هوا بیشتر شود. در نتیجه، سرعت واکنش سوختن آهن افزایش مییابد و شعلهور شدن آهن سریعتر اتفاق میافتد.

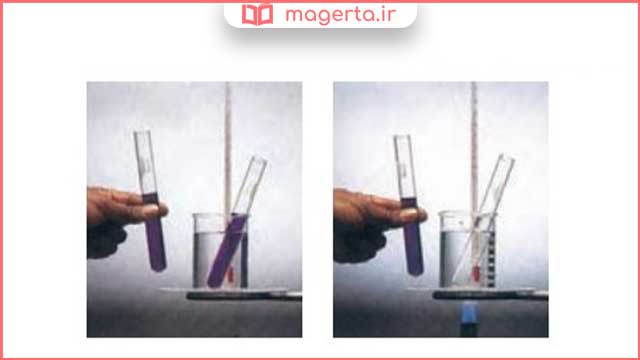
پ) محلول بنفش رنگ پتاسیم پرمنگنات با یک اسید آلی در دمای اتاق به کندی واکنش میدهد، اما با گرم شدن، محلول به سرعت بی رنگ میشود.
پاسخ: با افزایش دما سرعت واکنش افزایش می یابد، به همین جهت سریع تر بی رنگ می شود.
پاسخ دیگر: اثر دما روی سرعت واکنش، با گرم شدن محلول و افزایش دما، سرعت واکنش افزایش مییابد.
ت) الیاف آهن داغ و سرخ شده در هوا نمیسوزد، در حالی که همان مقدار الیاف آهن داغ و سرخ شده در یک ارلن پر از اکسیژن میسوزد.
پاسخ: با افزایش غلظت سرعت واکنش افزایش می یابد.، به همین جهت الیاف آهن در اکسیژن خالص با سرعت بیش تری واکنش می دهند و نور و گرمای بیش تری ایجاد می نمایند.
پاسخ دیگر: اثر غلظت بر سرعت واکنشهای شیمیایی به این صورت است که هرچه غلظت اولیه واکنشدهندهها بالاتر باشد، سرعت واکنش نیز افزایش مییابد.

ث) محلول هیدروژن پراکسید در دمای اتاق به کندی تجزیه شده و گاز اکسیژن تولید میکند، در حالی که افزودن دو قطره از محلول پتاسیم یدید، سرعت واکنش را به طور چشمگیری افزایش میدهد.
پاسخ: کاتالیزگر سرعت واکنش را افزایش می دهد، به همین جهت با افزایش پتاسیم یدید که نقش کاتالیزگر را دارد سرعت خروج گاز اکسیژن افزایش می یابد.
پاسخ دیگر: افزودن کاتالیزگر به مواد واکنشدهنده کاتالیزگر ماده است که بدون آن که خود به مصرف برسد، سبب افزایش سرعت واکنشهای شیمیایی میشود.

قبلی: جواب کاوش کنید صفحه ۸۰ و ۸۱ و ۸۲ شیمی یازدهم
جواب خود را بیازمایید صفحه ۷۸ شیمی یازدهم
جواب خود را بیازمایید صفحه ۷۶ و ۷۷ شیمی یازدهم
جواب در میان تارنماها صفحه ۷۴ شیمی یازدهم
جواب خود را بیازمایید صفحه ۷۳ و ۷۴ شیمی یازدهم
توجه: شما دانش آموز پایه یازدهم رشته های نظری ریاضی فیزیک و تجربی می توانید برای دسترسی سریع و آسان تر به جواب تمرینات و سوالات فصل های اول و دوم و سوم کتاب شیمی یازدهم متوسطه دوم ، در انتهای عنوان خود عبارت «ماگرتا» را نیز در گوگل جستجو کنید.
✅ در انتها امیدواریم که مقاله توضیح و جواب سوال های خودرابیازمایید صفحه ۸۲ و ۸۳ فصل دوم شیمی یازدهم تجربی و ریاضی ؛ برای شما دانش آموزان عزیز مفید بوده باشد. سوالات خود را در بخش نظرات بیان کنید.















