جواب تمرین های دوره ای صفحه ۹۶ و ۹۷ و ۹۸ فصل ۲ دوم شیمی یازدهم ؛ در این مقاله به پاسخ و جواب سوالات تمرین های دوره ای صفحه ی 96 و 97 و 98 فصل 2 دو قدر هدایای زمینی را بدانیم کتاب شیمی یازدهم تجربی و ریاضی فیزیک متوسطه دوم پرداخته ایم. در ادامه با بخش آموزش و پرورش ماگرتا همراه ما باشید.
بعدی: جواب خود را بیازمایید صفحه ۱۰۱ شیمی یازدهم
جواب در میان تارنماها صفحه ۱۰۲ شیمی یازدهم
جواب باهم بیندیشیم صفحه ۱۰۳ و ۱۰۴ شیمی یازدهم
جواب خود را بیازمایید صفحه ۱۰۶ شیمی یازدهم
جواب خود را بیازمایید صفحه ۱۰۹ شیمی یازدهم

پاسخ و حل تمرین های دوره ای فصل ۲ دوم شیمی یازدهم صفحه ۹۶ و ۹۷ و ۹۸
۱) اغلب ورزشکاران برای درمان آسیب دیدگیهای خود از بستههایی استفاده میکنند که به سرعت گرما را انتقال میدهند. اساس کار این بستهها، انحلال برخی ترکیبهای یونی در آب است. با توجه به معادلههای ترموشیمیایی زیر به پرسشهای مطرح شده پاسخ دهید:
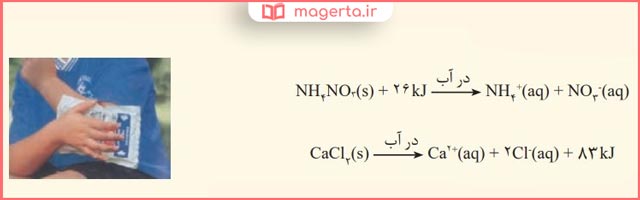
الف) کدام فرایند انحلال برای سرد کردن محل آسیب دیدگی مناسب است؟ چرا؟
پاسخ: واکنش اول(انحلال آمونیوم نیترات در آب)؛ چون گرماگیر است و با جذب گرما از محل آسیبدیده آن را سرد میکند.
ب) از انحلال کامل 2/22g کلسیم کلرید خشک در آب چند کیلوژول گرما آزاد میشود؟
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

۲) چربی ذخیره شده در کوهان شتر هنگام اکسایش افزون بر آب مورد نیاز، انرژی لازم برای فعالیتهای جانور را نیز تأمین میکند. واکنش ترموشیمیایی آن به صورت زیر است:
2C57H110O6(s) + 163O2(g) → 114CO2(g) + 110H2O(l) ، ΔH = -75520 kJ
حساب کنید از اکسایش هر کیلوگرم چربی، چند کیلوژول انرژی آزاد میشود؟
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

۳) کلسترول، یکی از مواد آلی موجود در غذاهای جانوری است که مقدار اضافی آن در دیواره رگها رسوب میکند، فرایندی که منجر به گرفتگی رگها و سکته میشود. با توجه به ساختار آن به پرسشهای مطرح شده پاسخ دهید.
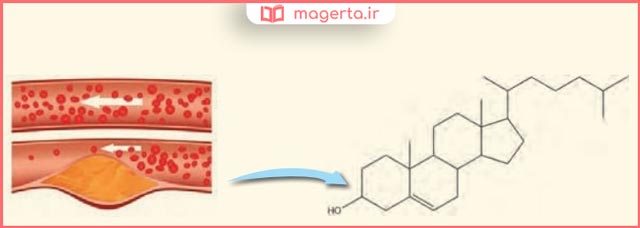
الف) توضیح دهید چرا شیمیدانها آن را یک الکل سیر نشده میدانند؟
پاسخ: چون در ساختار این مولکول، علاوه بر گروه عاملی الکلی (هیدروکسیل) یک پیوند دوگانه کربن کربن وجود دارد.
ب) با توجه به جدول شماره ۳، در شرایط یکسان کدام پیوندهای اشتراکی یگانه در ساختار کلسترول آسانتر شکسته میشود؟ چرا؟
پاسخ: در ساختار کلسترول، پیوندهای یگانه به صورت زیر میباشد:
[C−O ، C−C ، C−H ، O−H]
که به ترتیب از راست به چپ، دارای آنتالپیهای پیوند 463 ، 413 ، 348 و 380 کیلوژول بر مول میباشند. بنابراین پیوند C−C راحتتر شکسته میشود.
پاسخ دیگر: با توجه به مقادیر آنتالپی پیوند در جدول شماره 3، پیوند ساده کربن-کربن مقدار انرژی کمتری برای شکسته شدن نیاز دارد و آسانتر شکسته میشود.
۴) از مصرف هر گرم آلومینیم در واکنش ترمیت، 15/24kJ گرما آزاد میشود.
2Al(s) + Fe2O3(s) → Al2O3(s) + 2Fe(l)
الف) این مقدار گرما، دمای صد گرم آب خالص را چند درجه سلسیوس افزایش میدهد؟
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

ب) ΔH واکنش ترمیت را حساب کنید.
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

۵) با توجه به واکنش ترموشیمیایی: H2(g) + I2(s) + 53kJ → 2HI(g)، آنتالپی واکنش H2(g) + I2(s) → 2HI(g) را حساب کنید. راهنمایی: آنتالپی فرازش (تصعید) یُد را 62/5kJmol-1 در نظر بگیرید.
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

۶) شکل زیر واکنش میان گاز هیدروژن و بخار بنفش رنگ ید را در دمای معینی نشان میدهد.
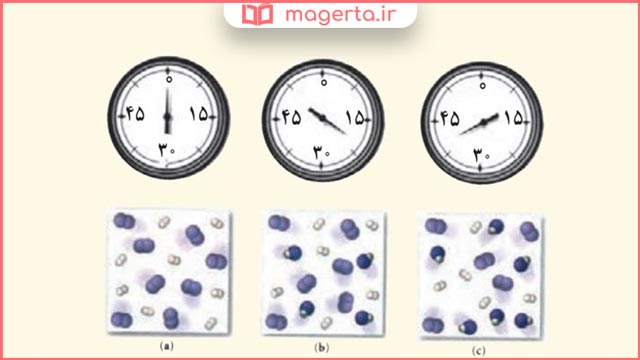
اگر هر ذره هم ارز با 0/1 مول از ماده و سامانه دو لیتری باشد، سرعت واکنش را پس از 20 دقیقه (b) و پس از 40 دقیقه (c) بر حسب mol L-1h-1 حساب و با یکدیگر مقایسه کنید.
پاسخ: از آنجا که زمان بر حسب min داده و بر حسب h خواسته شده است، بنابراین min را به h تبدیل می کنیم:
H2(g) + I2 → 2HI(g)
| c | b | a | ظرف / مولکول |
|---|---|---|---|
| 0/5 | 0/6 | 0/8 | H2 |
| 0/5 | 0/6 | 0/8 | I2 |
| 0/6 | 0/4 | 0 | HI |
ادامه پاسخ: در تصویر زیر می توانید ادامه پاسخ این پرسش را مشاهده کنید:

۷) ΔH واکنش را با استفاده از:
الف) جدول ۲ و ۳ حساب کنید.
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

ب) آنتالپی سوختن اتن، اتان و هیدروژن که به ترتیب برابر با ، 1410- ، 1560- و 286- کیلو ژول بر مول است، حساب کنید.
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

پ) ΔH محاسبه شده از کدام قسمت را برای یک گزارش علمی انتخاب میکنید؟ توضیح دهید.
پاسخ: محاسبات نشان میدهد که مقدار H∆ محاسبه شده به روش آنتالپی پیوند با مقدار اندازهگیری شده به روش تجربی تفاوت دارد و با خطای بیشتری همراه است. بنابراین آنتالپی واکنش بر حسب واکنش سوختن که خطای کمتری دارد انتخاب میشود.
۸) با توجه به جدول زیر به پرسشهای مطرح شده پاسخ دهید.
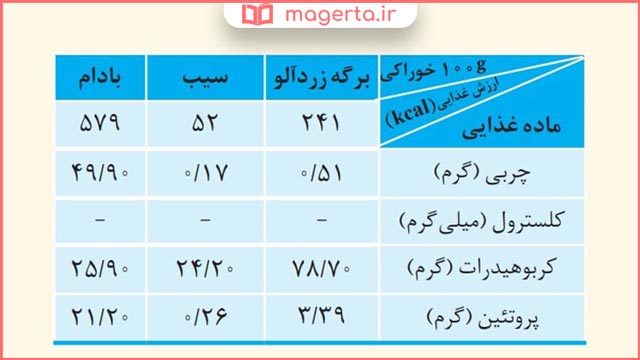
الف) اگر بدن فردی نیاز فوری و ضروری به تأمین انرژی داشته باشد، کدام خوراکی را پیشنهاد میکنید؟ چرا؟
پاسخ: برگه زردآلو. چون مقدار کربوهیدرات موجود در آن بیشتر است و زودتر تولید انرژی میکند.
ب) مصرف کدام خوراکی را برای فعالیتهای فیزیکی که در مدت طولانی تری انجام میشوند، مناسب میدانید؟ توضیح دهید.
پاسخ: بادام زمینی. زیرا میزان چربی موجود در آن بیشتر است و چربیها در مدت زمان طولانیتری در سوخت و ساز شرکت میکنند و کم کم انرژی خود را از دست میدهند.
پ) اگر یک فرد 70 کیلوگرمی، 25 گرم بادام خورده باشد، برای مصرف انرژی حاصل از آن چه مدت باید پیاده روی کند؟آهنگ مصرف انرژی در پیاده روی را 190kcal h-1 در نظر بگیرید.
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

٩- با توجه به اطلاعات داده شده، آنتالپی واکنش زیر را حساب کنید.
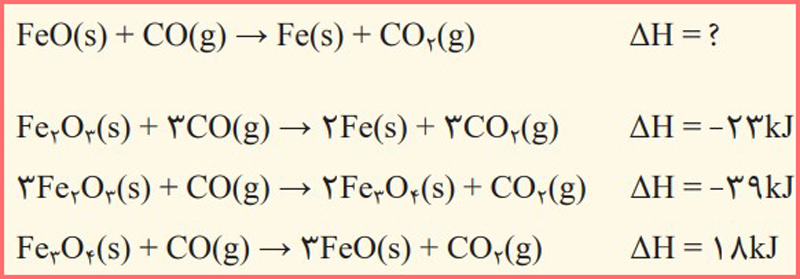
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:

۱۰- در نمودار زیر، منحنی C مربوط به واکنش 0/5 گرم نوار منیزمی با مقدار کافی از هیدروکلریک اسید در دمای اتاق
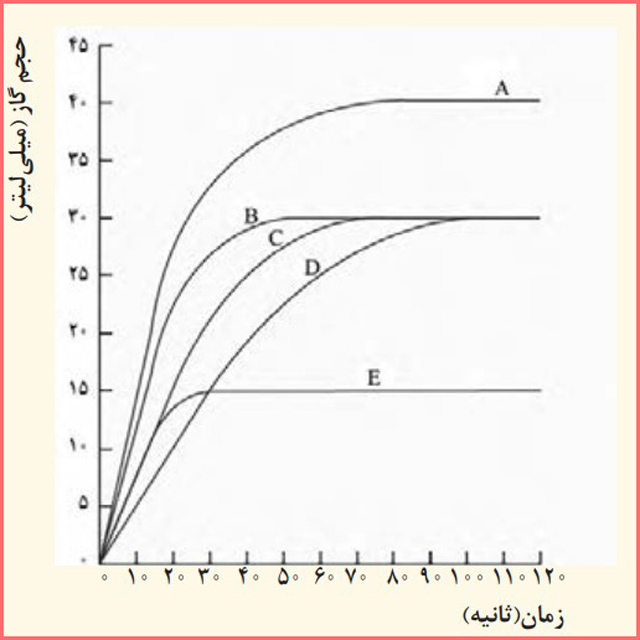
الف) سرعت واکنش را برای آزمایشهای C و D برحسب لیتر بر ساعت حساب کنید.
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:
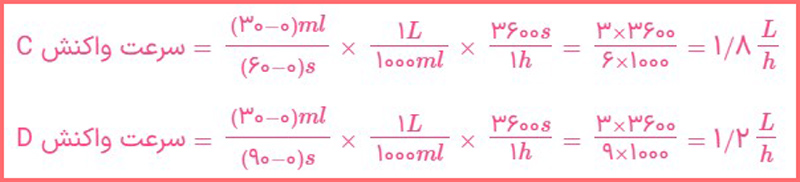
ب) کدام منحنی مربوط به واکنشی است که در آن 0/5 گرم پودر منیزمی به جای نوار منیزمی استفاده شده است؟ (بقیه شرایط واکنش تغییر نکرده است.) دلیل خود را توضیح دهید.
پاسخ: واکنش A؛ به این دلیل که در حالت پودر بودن، اتم های واکنش دهنده در تماس بیشتری با یکدیگر هستند و بنابراین سرعت واکنش بیشتر می شود، ولی در حالت نوار بودن، ابتدا اتم های روی روکش نوار باید واکنش دهند تا تماس با اتم های دیگر واکنش دهنده منیزیم اتفاق بیفتد و این خود نیز زمان بر می باشد و سرعت واکنش کمتر از حالت پودری می شود.
پ) کدام منحنی مربوط به واکنش 0/5 گرم نوار منیزمی با مقدار کافی از هیدروکلریک اسید در دمای 5 درجه سلسیوس است؟ چرا؟
پاسخ: واکنش E؛ زیرا هر چه دمای پایین باشد، سرعت حرکت اتم های واکنش دهنده کمتر می باشد و برای تماس بین اتم های واکنش دهنده زمان بیشتری نیاز می باشد و واکنش با سرعت کمتری اتفاق می افتد. همچنین به این دلیل که برای سرعت بخشیدن به واکنش نیاز به انرژی بیشتری می باشد و در دمای پایین، انرژی واکنش دهنده ها کمتر می باشد، انرژی بوجود آمده بعد از ترکیب واکنش دهنده ها صرف گرم کردن و انرژی دادن به اتم های واکنش دهنده دیگر می شود تا واکنش صورت پذیرد که این خود باعث می شود سرعت واکنش در دمای پایین، کمتر شود.
قبلی: جواب خود را بیازمایید صفحه ۹۵ شیمی یازدهم
جواب باهم بیندیشیم صفحه ۹۲ و ۹۳ شیمی یازدهم
جواب خود را بیازمایید صفحه ۹۱ و ۹۲ شیمی یازدهم
جواب در میان تارنماها صفحه ۹۱ شیمی یازدهم
جواب خود را بیازمایید صفحه ۸۹ و ۹۰ شیمی یازدهم
توجه: شما دانش آموز پایه یازدهم رشته های نظری ریاضی فیزیک و تجربی می توانید برای دسترسی سریع و آسان تر به جواب تمرینات و سوالات فصل های اول و دوم و سوم کتاب شیمی یازدهم متوسطه دوم ، در انتهای عنوان خود عبارت «ماگرتا» را نیز در گوگل جستجو کنید.
✅ در انتها امیدواریم که مقاله توضیح و جواب سوال های تمرین های دوره ای صفحه ۹۶ و ۹۷ و ۹۸ فصل ۲ دوم شیمی یازدهم تجربی و ریاضی ؛ برای شما دانش آموزان عزیز مفید بوده باشد. سوالات خود را در بخش نظرات بیان کنید.
















متشکر ، دو سوال آخر نبود
مثل سوال آخر تمرین دوره ای فصل اول
لطفاً بروز کنید
ممنون!
ممنون
و خسته نباشید
ممنون.
دو سوال آخر نیست.
عالی بود
عالی بود
متشکرم
خوب بود ممنون از شما
خوب بود
مفید بود