جواب باهم بیندیشیم صفحه ۸۰ و ۸۱ شیمی دوازدهم تجربی و ریاضی ؛ در این مقاله به پاسخ و جواب سوالات تمرین با هم بیندیشیم صفحه ی 80 و 81 فصل سوم شیمی جلوه ای از هنر ، زیبایی و ماندگاری کتاب شیمی دوازدهم تجربی و ریاضی فیزیک متوسطه دوم پرداخته ایم. در ادامه با بخش آموزش و پرورش ماگرتا همراه ما باشید.
بعدی: جواب خود را بیازمایید صفحه ۸۲ و ۸۳ شیمی دوازدهم
جواب با هم بیندیشیم صفحه ۸۴ شیمی دوازدهم
جواب خود را بیازمایید صفحه ۸۶ شیمی دوازدهم
جواب باهم بیندیشیم صفحه ۸۷ شیمی دوازدهم
جواب تمرین های دوره ای فصل سوم شیمی دوازدهم

پاسخ و حل با هم بیندیشیم صفحه ۸۰ و ۸۱ شیمی دوازدهم تجربی و ریاضی
۱- توضیح دهید چرا برای توصیف ترکیبهای یونی در منابع علمی معتبر هیچ گاه واژههایی مانند مولکول و فرمول مولکولی به کار نمیرود؟
پاسخ: شبکه بلور جامدهای یونی از کنار هم قرار گرفتن یون های مثبت و منفی ساخته شده، بنابراین واحدهای مجزایی به نام مولکول ندارند. بنابراین نمیتوان از کلمات مولکول و فرمول مولکولی برای آنها استفاده کرد.
پاسخ دیگر: در شبکه بلوری ترکیب های یونی، آرایش یون ها در سرتاسر شبکه از یک الگوی تکراری پیروی می کند. هر کاتیون و آنیون عدد کوئورد دیناسیون معینی دارد به طوری که در ساختار آن ها مولکول های مجزا وجود ندارد.
۲- جدول زیر اندازۀ شعاع برخی یونهای متداول را در مقایسه با اندازۀ اتم سازندۀ آنها نشان میدهد. در مورد این جدول با یکدیگر گفتوگو کنید و روندهای موجود در آن را توضیح دهید.
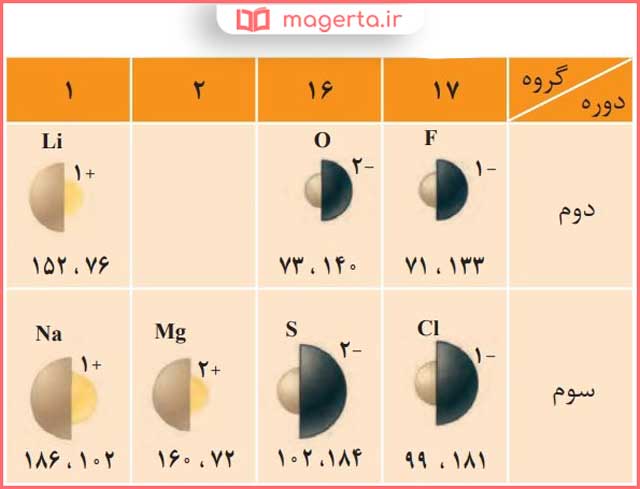
پاسخ: در هر گروه از بالا به پایین با افزایش عدد اتمی، لایههای الکترونی افزایش یافته و شعاع اتمی افزایش مییابد.
در هر گروه از بالا به پایین شعاع یونی نیز افزایش مییابد.
در هر دوره ازچپ به راست با افزایش عدد اتمی، لایههای الکترونی ثابت مانده و به دلیل افزایش جاذبهٔ هسته روی الکترونهای بیرونیترین لایه، شعاع اتمی کاهش مییابد.
در هر دوره از چپ به راست، شعاع کاتیونها نسبت به هم کاهش مییابد.
در هر دوره از چپ به راست، شعاع آنیونها نسبت به هم افزایش مییابد.
در هر دوره از چپ به راست، شعاع آنیونها بزرگتر از شعاع کاتیونهاست.
در کاتیونها، هرچه بارکاتیون ↓ (کاهش یابد) ⇐ شعاع کاتیون ↑ (افزایش مییابد)
در آنیونها، هرچه بار آنیون ↓ (کاهش یابد) ⇐ شعاع آنیون ↑ (افزایش مییابد)
شعاع هر کاتیون از اتم سازندهٔ خودش، کمتر است.
شعاع هر آنیون از اتم سازندهٔ خودش، بیشتر است.
پاسخ دیگر: در همه گروه های عناصر اصلی شعاع اتمی و یون پایدار آنها از بالا به پایین افزایش می یابد. در عناصر هم دوره هرچه بار الکتریکی کاتیون بیش تر باشد، شعاع آن کوچکتر و هرچه بار الکتریکی آنیون بیش تر باشد، شعاع آن بزرگتر است.
۳- اگر هریون را کرهای باردار در نظر بگیرید، چگالی بار هم ارز با نسبت بار به حجم آن است. کمیتی که میتواند برای مقایسۀ میزان بر همکنش میان یونها به کار رود. نسبت سادهتری که میتوان به کاربرد، نسبت مقدار بار یون به شعاع آن است. با این توصیف جدول زیر را کامل کنید و به پرسشها پاسخ دهید.
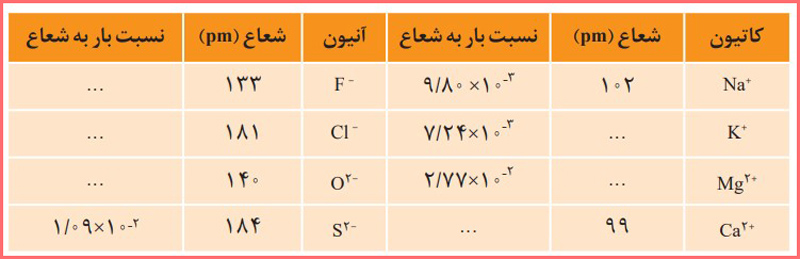
پاسخ: در تصویر زیر می توانید جدول کامل شده را مشاهده کنید:
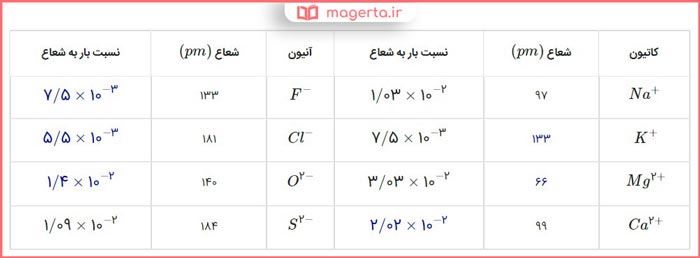
آ) چگالی بار کدام کاتیون کمتر و کدام یک بیشتر است؟ چرا؟
پاسخ: یون پتاسیم (+K) کمترین و یون منیزیم (+Mg2) بیشترین چگالی بار را در بین کاتیونها دارند، زیرا هر چه نسبت بار به شعاع یون کوچکتر باشد، چگالی بار آن کمتر است و برعکس.
ب) چگالی بار کدام آنیون کمتر و کدام یک بیشتر است؟ چرا؟
پاسخ: چگالی بار آنیون کلرید (–Cl) کمتر و چگالی بار آنیون اکسید (–S2) بیشتر است، زیرا هرچه بار آنیون بیشتر شود، شعاع آن بیشتر شده و نسبت بار به شعاع افزایش مییابد. اگر بار آنیونها، با هم برابر باشد، چگالی بار آنیونی بیشتر است که شعاع کوچکتری دارد.
پ) پیش بینی کنید نیروی جاذبه میان کدام کاتیون با کدام آنیون از همه قویتر است؟ چرا؟
پاسخ: نیروی جاذبه منیزیم (+Mg2) و اکسید (–O2) میان بیشتر است. نیروی جاذبهٔ بین یونها با بار یونها رابطهٔ مستقیم و با شعاع یونها رابطهٔ عکس دارد.
ت) پیش بینی کنید نیروی جاذبه میان کدام کاتیون با کدام آنیون از همه ضعیفتر است؟ چرا؟
پاسخ: نیروی جاذبه پتاسیم (+K) و کلرید (–Cl) میان کمتر است. نیروی جاذبهٔ بین یونها با بار یونها رابطهٔ مستقیم و با شعاع یونها رابطهٔ عکس دارد.
قبلی: جواب باهم بیندیشیم صفحه ۷۸ شیمی دوازدهم
جواب خود را بیازمایید صفحه ۷۶ و ۷۷ شیمی دوازدهم
جواب خود را بیازمایید صفحه ۷۴ شیمی دوازدهم
جواب کاوش کنید صفحه ۷۳ شیمی دوازدهم
جواب در میان تارنماها صفحه ۷۳ شیمی دوازدهم
توجه: شما دانش آموز پایه دوازدهم رشته های نظری ریاضی فیزیک و تجربی می توانید برای دسترسی سریع و آسان تر به جواب تمرینات و سوالات فصل های اول تا چهارم کتاب شیمی دوازدهم متوسطه دوم ، در انتهای عنوان خود عبارت «ماگرتا» را نیز در گوگل جستجو کنید.
✅ در انتها امیدواریم که مقاله توضیح و جواب سوال های باهم بیندیشیم صفحه ۸۰ و ۸۱ فصل سوم شیمی دوازدهم تجربی و ریاضی ؛ برای شما دانش آموزان عزیز مفید بوده باشد. سوالات خود را در بخش نظرات بیان کنید.















عالی