جواب تمرین های دوره ای صفحه ۶۳ و ۶۴ فصل دوم شیمی دوازدهم ؛ در این مقاله به پاسخ و جواب سوالات تمرین های دوره ای صفحه ی 63 و 64 فصل 2 دوم آسایش و رفاه در سایه شیمی کتاب شیمی دوازدهم تجربی و ریاضی فیزیک متوسطه دوم پرداخته ایم. در ادامه با بخش آموزش و پرورش ماگرتا همراه ما باشید.
همچنین بخوانید: جواب خود را بیازمایید صفحه ۶۲ شیمی دوازدهم فصل دوم

پاسخ و حل تمرین های دوره ای فصل ۲ دوم شیمی دوازدهم صفحه ۶۳ و ۶۴
۱- برای هر یک از جملههای زیر، دلیلی بنویسید.
آ) فلز پلاتین را میتوان در بخشهای مختلف بدن هنگام جراحی به کار برد.
پاسخ: فلز پلاتین جزوفلزهای نجیب است. این فلز به دلیل داشتن E۰ بزرگ، تمایلی برای از دست دادن الکترون و شرکت در واکنشهای شیمیایی ندارد، بنابراین با الکترولیتها مواد موجود در بدن واکنش نمیدهد.
ب) فلوئور، اكسندهترین عنصر در جدول دورهای است.
پاسخ: فلوئور به عنوان فعالترین نافلز جدول دورهای تمایلی به دادن الکترون ندارد، بلکه تمایل بسیار زیاد برای گرفتن الکترون و کاهش یافتن دارد، بنابراین قدرت اکسندگی زیادی هم دارد.
E۰(F2/F) = +2/8 V
پ) عدد اکسایش اکسیژن در OF2 برابر با 2+ است.
پاسخ: در تصویر زیر می توانید پاسخ این بخش را مشاهده کنید:
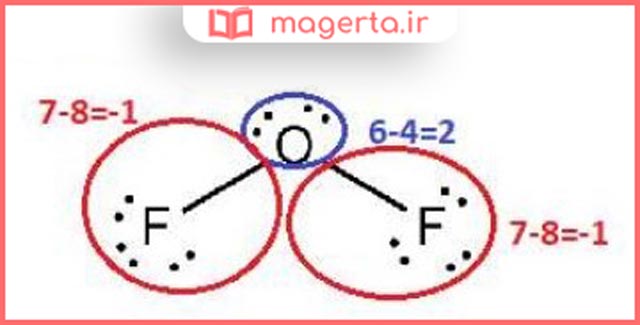
۲- با مراجعه به جدول 1 ،توضیح دهید کدام نمودار تغییر غلظت یونها را در سلول گالوانی روی ــ مس نشان میدهد.
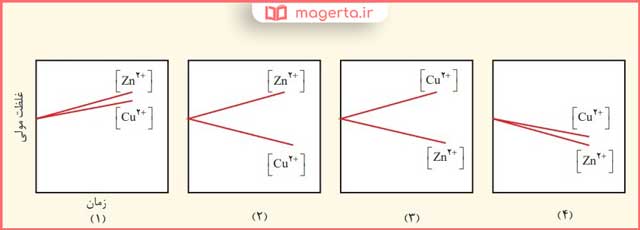
پاسخ: در نمودار شماره (۲)، پتانسیل کاهشی مس بیشتر از روی است، بنابراین در سلول گالوانی مس از نوع کاتد و روی از نوع آند است. با گذشت زمان از غلظت یونهای دو بار مثبت مس در کاتد کم می شود و بر غلظت یونهای رو دو بار مثبت در آند افزوده می شود.
۳- emf سلولی که واکنش زیر در آن رخ میدهد برابر با 1/98V است. E۰ نیم سلول A را حساب کرده و با مراجعه به جدول مشخص کنید A کدام فلز است؟
A(s) + 2Ag+(aq) → A2+(aq) + 2Ag(s)
پاسخ: در تصویر زیر می توانید پاسخ این بخش را مشاهده کنید:

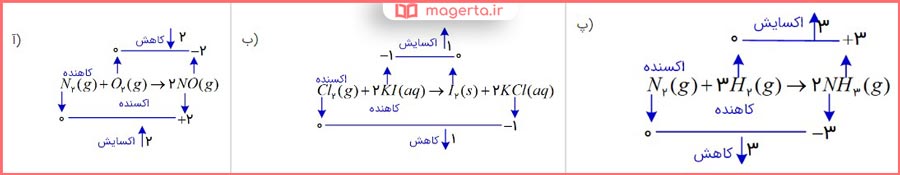
۴- عدد اکسایش اتم نشان داده شده با ستاره را مشخص کنید.
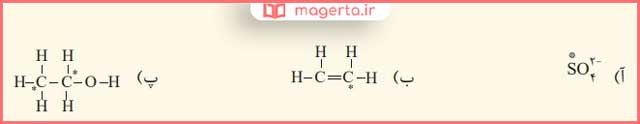
پاسخ: در تصویر زیر می توانید پاسخ این بخش را مشاهده کنید:
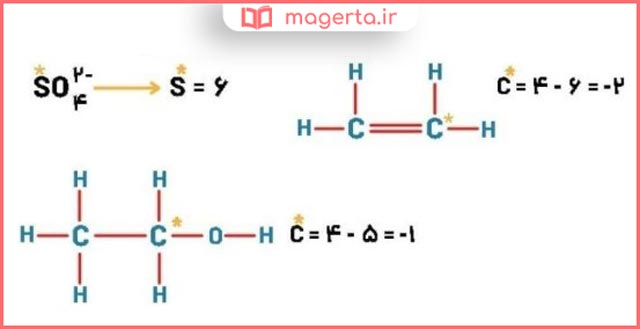
۵- در هر یک از واکنشهای زیر گونههای اکسنده و کاهنده را مشخص کنید.

پاسخ: در تصویر زیر می توانید پاسخ این بخش را مشاهده کنید:
۶- باتریهای روی ــ نقره از جمله باتریهای دگمهای هستند که در آنها واکنش زیر انجام میشود.
Zn(s) + Ag2O(s) → ZnO(s) + 2Ag(s)
آ) گونههای اکسنده و کاهنده را در آن مشخص کنید.
پاسخ: اکسنده: نقره (Ag)
کاهنده: روی (Zn)
ب) آند و کاتد را در این باتری مشخص کنید.
پاسخ: آند: روی (Zn) – کاتد: نقره (Ag)
۷) با توجه به جدول زیر به پرسشها پاسخ دهید.
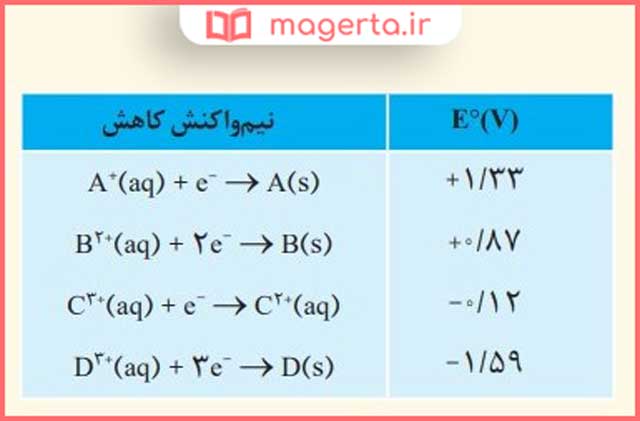
آ) کدام گونه قویترین و کدام ضعیفترین اکسنده است؟
پاسخ: قویترین اکسنده: A+(aq) چون بیشترین E۰ را دارد.
ضعیفترین اکسنده: D3+(aq) چون کمترین E۰ را دارد.
ب) کدام گونه قویترین و کدام ضعیفترین کاهنده است؟
پاسخ: قویترین کاهنده: D3+(aq) – هر چه پتانسیل کاهشی یک نیم واکنش کمتر باشد، گونه سمت راست آن کاهندهی قوی تری است.
ضعیفترین کاهنده: A+(aq) – هر چه پتانسیل کاهشی یک نیم واکنش بزرگتر باشد، گونه سمت راست آن کاهنده ضعیف تری است.
پ) کدام گونه(ها) میتوانند +C2 را اکسید کنند؟
پاسخ: هر گونهای که پتانسیل کاهشی بیشتری نسبت به نیم واکنش کاهش +C3 داشته باشد می تواند +C2 را اکسید کند. بنابراین گونههای A+(aq) و B2+(aq) میتوانند +C2 را اکسید کنند.
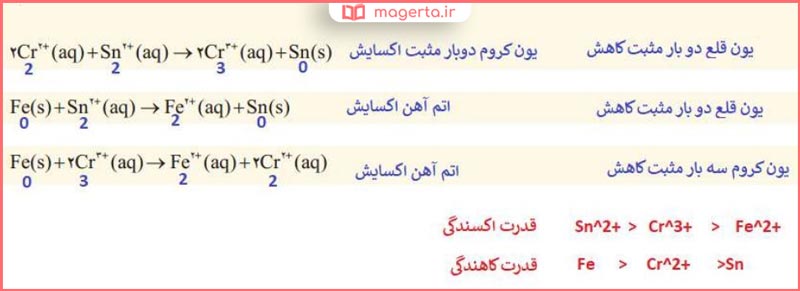
۸- با توجه به واکنشهای زیر که به طور طبیعی انجام میشوند، گونههای کاهنده و گونههای اکسنده را بر حسب کاهش قدرت مرتب کنید؟

پاسخ: در تصویر زیر می توانید پاسخ این بخش را مشاهده کنید:
۹- با توجه به جدول پتانسیلهای کاهشی استاندارد توضیح دهید محلول هیدروکلریک اسید را در کدام ظرف (مسی یا آهنی) می توان نگه داشت؟
پاسخ: ظرف مسی مناسب است. به طور کلی برای نگه داری محلولها جنس ظرف باید از فلزی انتخاب شود که جایگاه آن در جدول پتانسیل کاهشی استاندارد بالاتر از کاتیون موجود در محلول باشد، پس برای نگهداری محلول رقیق اسیدها باید ظرفی را انتخاب کرد که E۰ آن را بالاتر از هیدروژن باشد. (0 < E۰)
۱۰- شیمیدانها در برخی سلولهای الکتروشیمیایی برای انجام واکنش اکسایش ــ کاهش از نور بهره میبرند و آنها را سلول نور الکتروشیمیایی مینامند. در نمونهای از آنها که برای تهیه گاز هیدروژن از آب به کار میرود، با توجه به نیم واکنشهای زیر:

آ) نیم سلول آند و کاتد را مشخص و emf سلول را حساب کنید.
پاسخ: SiO2(s) + 4H+(aq) + 4e– → Si(s) + 2H2O(l) :نیم سلول آند
2H2O(l) + 2e– → H2(g) + 2OH–(aq) :نیم سلول کاتد
emf = 0/83 – (-0/84) = 0/01 V
ب) یافتههای تجربی نشان میدهند که افزون بر emf، بازده و سرعت انجام واکنش در این سلول پایین است، با این توصیف چرا برخی استفاده از آنها را برای تهیه گاز هیدروژن مناسب میدانند؟
پاسخ: زیرا گاز H2 (هیدروژن)، گاز خطرناکی است و تحت کنترل تولید می شود.
همچنین بخوانید: جواب خود را بیازمایید صفحه ۶۰ و ۶۱ شیمی دوازدهم
و
جواب خود را بیازمایید صفحه ۵۹ شیمی دوازدهم
توجه: شما دانش آموز پایه دوازدهم رشته های نظری ریاضی فیزیک و تجربی می توانید برای دسترسی سریع و آسان تر به جواب تمرینات و سوالات فصل های اول تا چهارم کتاب شیمی دوازدهم متوسطه دوم ، در انتهای عنوان خود عبارت «ماگرتا» را نیز در گوگل جستجو کنید.
✅ در انتها امیدواریم که مقاله توضیح و جواب سوال های تمرین های دوره ای صفحه ۶۳ و ۶۴ فصل دوم شیمی دوازدهم تجربی و ریاضی ؛ برای شما دانش آموزان عزیز مفید بوده باشد. سوالات خود را در بخش نظرات بیان کنید.












