جواب باهم بیندیشیم صفحه ۵۷ شیمی دوازدهم تجربی و ریاضی ؛ در این مقاله به پاسخ و جواب سوالات تمرین با هم بیندیشیم صفحه ی 57 فصل دوم آسایش و رفاه در سایه شیمی کتاب شیمی دوازدهم تجربی و ریاضی فیزیک متوسطه دوم پرداخته ایم. در ادامه با بخش آموزش و پرورش ماگرتا همراه ما باشید.
همچنین بخوانید: جواب خود را بیازمایید صفحه ۵۵ و ۵۶ شیمی دوازدهم

پاسخ و حل با هم بیندیشیم صفحه ۵۷ شیمی دوازدهم تجربی و ریاضی
۱- با توجه به شکل های زیر، به پرسشهای مطرح شده پاسخ دهید.
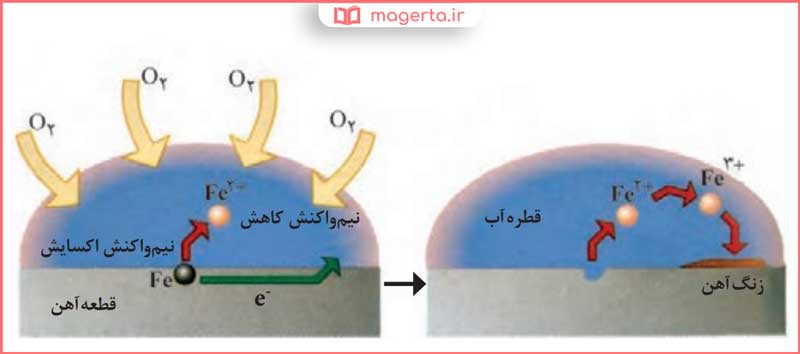
آ) چگونگی تشکیل زنگ آهن را توصیف کنید.
پاسخ: اگر به جرمی از آهن، به میزان کافی زمان بدهیم، در حضور آب و اکسیژن، به طور کامل به زنگ آهن تبدیل میشود. زنگ آهن در سطح خود به صورت پوسته پوسته و شکننده ظاهر میشود و هیچ حفاظتی را در برابر سطوح زیرین خود در برابر زنگ زدگی ایجاد نمیکند.
ب) هر یک از نیم واکنشها را موازنه کنید.
Fe(s) → Fe2+ (aq) + ……
O2(g) + H2O(l) + ……. → OH–(aq)
پاسخ: نیم واکنش های زیر:
2Fe(s) → 2Fe2+ (aq) + 4e–
O2(g) + 2H2O(l) + 4e– → 4OH–(aq)
پ) با توجه به اینکه زنگ آهن حاوی یون آهن (III) است، نیم واکنش اکسایش یون آهن (II) به یون آهن (III) را بنویسید.
پاسخ: Fe2+(aq) → Fe3+(aq) + e– نیم واکنش آندی
پ) فراورده نهایی خوردگی، زنگ آهن است. اگر فرمول شیمیایی آن را Fe(OH)3 در نظر بگیریم، معادله واکنش زیر را به روش وارسی موازنه کنید.
Fe(s) + H2O(l) + O2(g) → Fe(Oh)3(s)
پاسخ:
4Fe(s) + 6H2O(l) + 3O2(g) → 4Fe(OH)3(s)
۲- با توجه به نیم واکنشهای زیر توضیح دهید چرا :
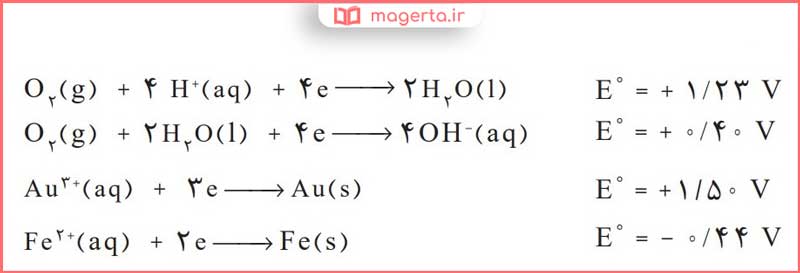
آ) خوردگی آهن در محیط اسیدی به میزان بیشتری رخ میدهد؟
پاسخ: پتانسیل کاهشی اکسیژن در محیط اسیدی بیشتر است، بنابراین سبب اکسایش و خوردگی بیشتر آهن میشود.
پاسخ دیگر: چون در محیط اسیدی غلظت یون H+(aq) زیاد است، با توجه به:
E۰(Fe2+/Fe) = – 0/44 و E۰(H+/H) = 0
متوجه میشویم که تمایل آهن به دادن الکترون بیشتر از H+(aq) است، پس Fe اکسایش بیشتری مییابد.
ب) با گذشت زمان فلز طلا در هوای مرطوب و حتی در اعماق دریا همچنان درخشان باقی میماند؟
پاسخ: پتانسیل کاهشی طلا در محیط مرطوب و اسیدی از اکسیژن بیشتر است، بنابراین واکنش نخواهد داد.
پاسخ دیگر: E۰ فلز طلا بالای H+(aq) E۰ در جدول سری الکتروشیمیایی قرار دارد، پس هیچگاه نمیتواند در رقابت برای دادن الکترون برنده شود در نتیجه هیچگاه اکسایش نمییابد.
همچنین بخوانید: جواب خود را بیازمایید صفحه ۵۴ شیمی دوازدهم
و
جواب خود را بیازمایید صفحه ۵۳ شیمی دوازدهم
توجه: شما دانش آموز پایه دوازدهم رشته های نظری ریاضی فیزیک و تجربی می توانید برای دسترسی سریع و آسان تر به جواب تمرینات و سوالات فصل های اول تا چهارم کتاب شیمی دوازدهم متوسطه دوم ، در انتهای عنوان خود عبارت «ماگرتا» را نیز در گوگل جستجو کنید.
✅ در انتها امیدواریم که مقاله توضیح و جواب سوال های باهم بیندیشیم صفحه ۵۷ فصل دوم شیمی دوازدهم تجربی و ریاضی ؛ برای شما دانش آموزان عزیز مفید بوده باشد. سوالات خود را در بخش نظرات بیان کنید.













بسیار عالی😊🦋،خیلی ممنون