جواب باهم بیندیشیم صفحه ۲۶ و ۲۷ شیمی دوازدهم تجربی و ریاضی ؛ در این مقاله به پاسخ و جواب سوالات تمرین با هم بیندیشیم صفحه ی 26 و 27 فصل اول مولکول ها در خدمت تندرستی کتاب شیمی دوازدهم تجربی و ریاضی فیزیک متوسطه دوم پرداخته ایم. در ادامه با بخش آموزش و پرورش ماگرتا همراه ما باشید.
بعدی: جواب خود را بیازمایید صفحه ۲۸ شیمی دوازدهم
جواب خود را بیازمایید صفحه ۲۹ و ۳۰ شیمی دوازدهم
جواب خود را بیازمایید صفحه ۳۲ شیمی دوازدهم
جواب تمرین های دوره ای فصل اول شیمی دوازدهم
جواب باهم بیندیشیم صفحه ۴۰ شیمی دوازدهم

پاسخ و حل با هم بیندیشیم صفحه ۲۶ و ۲۷ شیمی دوازدهم تجربی و ریاضی
۱- آزمایشهای دقیق نشان میدهند که آب خالص رسانایی الکتریکی ناچیزی دارد. این ویژگی بیانگر وجود مقدار بسیار کمی از یونهای هیدرونیوم و هیدروکسید است. در واقع در یک نمونه از آب خالص شمار بسیار ناچیزی از مولکولهای H2O به یونهای H+(aq) و H–(aq) یونیده میشوند. جالب این است که اندازهگیریها و یافتههای تجربی در دمای اتاق برای آب و محلولهای آبی رابطه زیر را تأیید میکنند:
[H+] [OH–] = 10-14
آ) غلظت یونهای هیدرونیوم و هیدروکسید را در دمای اتاق برای آب خالص حساب کنید.
پاسخ: مطابق معادله واکنش به ازای هر مولکول آب که یونیده می شود یک یون هیدرونیوم و یک یون هیدروکسید تولید خواهد شد. از این رو در آب خالص [–OH] = [+H] است. پس:
[H+] [OH–] = 10-14 → [H+]2 = 10-14 → [H+] = 10-7 = [OH–]
ب) PH آب خالص و محلولهای خنثی را در دمای 25C حساب کنید.
پاسخ: ماده (2) زیرا باعث افزایش غلظت یون هیدرونیوم در آب شده است.
PH = -log [H+] = -log10-7 = 7
۲- شکل زیر تغییر غلظت یونهای هیدرونیوم و هیدروکسید را هنگام افزودن هر یک از مواد 1 و 2 به آب خالص نشان میدهد. با توجه به آن به پرسشها پاسخ دهید.
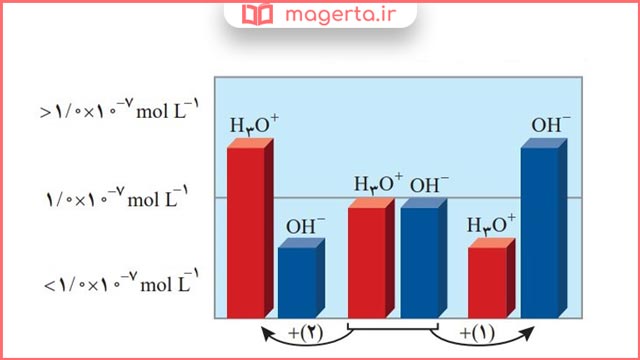
آ) کدام یک از مواد افزوده شده اسید آرنیوس است؟ چرا؟
پاسخ: ماده (2) – زیرا باعث افزایش غلظت یون هیدرونیوم (+H3O) در آب شده است.
ب) غلظت یونهای هیدرونیوم و هیدروکسید را در محلول بازی با یکدیگر مقایسه کنید.
پاسخ: در همه محلول های بازی غلظت یون هیدروکسید بیشتر از یون هیدرونیوم ( [+H3O] < [–OH] ) است.
پ) آیا میتوان گفت در محلولهای اسیدی، یون هیدروکسید وجود ندارد؟ توضیح دهید.
پاسخ: خیر – زیرا در همه محلول های آبی (اسیدی ، بازی یا خنثی) یون های هیدرونیوم و هیدروکسید وجود دارند اما مقدار آنها متفاوت است. به طوری که در محلول های اسیدی [–OH] < [+H] اما در محلولهای بازی [+H] < [–OH] است.
۳- گروهی از دانش آموزان برای نمایش تغییر غلظت یونهای هیدرونیوم و هیدروکسید در محلولهای آبی و دمای اتاق الگوی زیر را طراحی کردهاند. جاهای خالی را پر کنید و اساس کار آنها را توضیح دهید.
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:
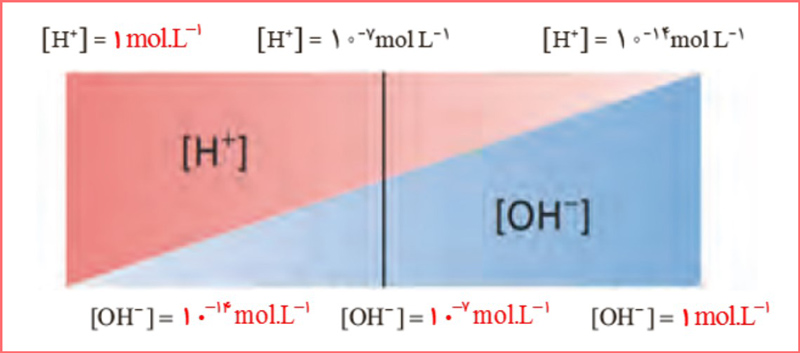
ادامه پاسخ: این طرح نشان می دهد که برای هر محلول آبی در دمای اتاق، 14-10 = [–OH] [+H] برقرار است و با افزایش غلظت یکی از غلظت دیگری کاسته می شود اما همواره در این دما، حاصلضرب غلظت این یون ها برابر با 14-10 است.
۴- در نمودار زیر، برای محلول آمونیاک، ستون نشان دهنده غلظت یون هیدروکسید و برای اسید معده، ستون نشان دهنده غلظت یون هیدرونیوم را رسم کنید.
پاسخ: در تصویر زیر می توانید پاسخ این پرسش را مشاهده کنید:
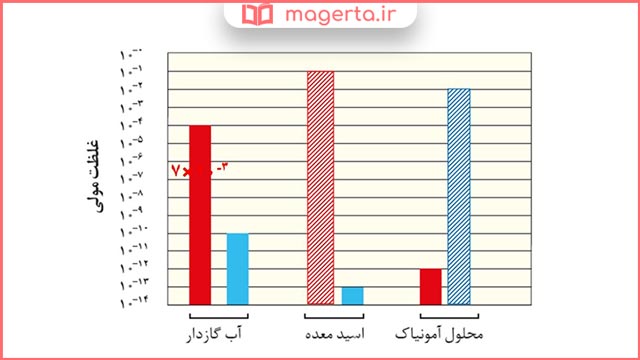
قبلی: جواب پیوند با ریاضی صفحه ۲۴ و ۲۵ شیمی دوازدهم
جواب خود را بیازمایید صفحه ۲۴ شیمی دوازدهم
جواب باهم بیندیشیم صفحه ۲۲ و ۲۳ شیمی دوازدهم
جواب کاوش کنید صفحه ۲۰ و ۲۱ شیمی دوازدهم
جواب خود را بیازمایید صفحه ۱۹ شیمی دوازدهم
توجه: شما دانش آموز پایه دوازدهم رشته های نظری ریاضی فیزیک و تجربی می توانید برای دسترسی سریع و آسان تر به جواب تمرینات و سوالات فصل های اول تا چهارم کتاب شیمی دوازدهم متوسطه دوم ، در انتهای عنوان خود عبارت «ماگرتا» را نیز در گوگل جستجو کنید.
✅ در انتها امیدواریم که مقاله توضیح و جواب سوال های باهم بیندیشیم صفحه ۲۶ و ۲۷ فصل اول شیمی دوازدهم تجربی و ریاضی ؛ برای شما دانش آموزان عزیز مفید بوده باشد. سوالات خود را در بخش نظرات بیان کنید.















